Tutkijat ovat kehittäneet uuden menetelmän, jossa tekoälyä käytetään ohjaamaan ionisoituvien lipidien muotoilua täsmäkohdennetussa mRNA-toimituksessa. Tämä innovaatio voi merkittävästi parantaa mRNA-rokotteiden ja -hoitojen tehokkuutta ja kohdentamista tiettyihin elimiin.
Tutkimus lipidien avaruusrakenteesta
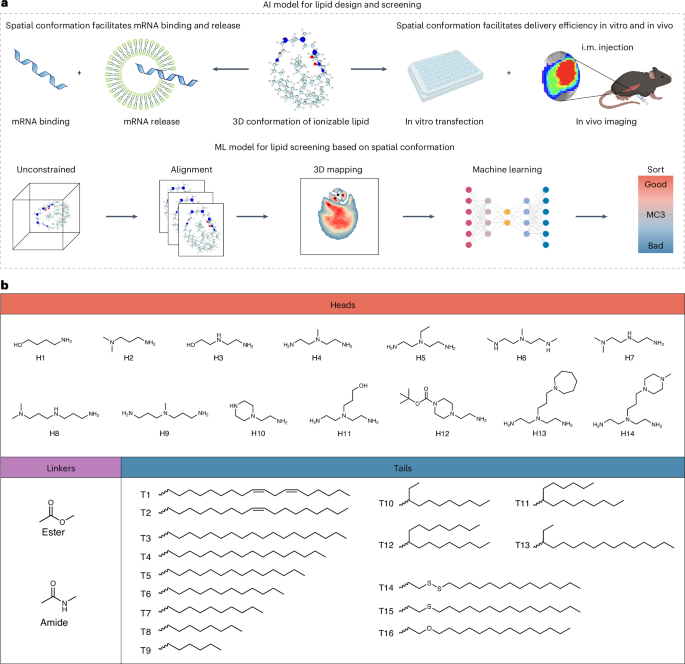
Ionisoituvien lipidien rooli mRNA-toimituksessa on ollut tiedossa, mutta niiden avaruusrakenteen vaikutus elinkohdentamiseen ja endosomaaliseen pakoon on ollut vähemmän tutkittu. Tutkijat loivat laajan kirjaston lipidejä, joissa oli erilaisia aminohappopäitä, hajoavia linkkejä ja hydrofobisia häntiä, muodostaen ainutlaatuisia kolmiulotteisia rakenteita. Molekyylidynamiikan simulaatiot paljastivat, miten nämä lipidit käyttäytyvät orgaanis-vesivaiheiden siirtymissä. Kokeellinen validointi osoitti, että lipidien pää- ja häntäjärjestelyt ovat keskeisiä toimitustehokkuudelle ja elinspesifisyydelle.
Tekoälyn rooli lipidien valinnassa
Lipidien dynaamiset konformaatiotiedot muunnettiin 2D-tiheyden kuviksi, jotka koulutettiin koneoppimismalleille lipidien valintaa varten. Tekoälyn ohjaamat kandidaatit, erityisesti lipidi P1, omaksuivat vakaita kolmihaara-kartiomaisia konformaatiota, jotka edistivät IgM-proteiinikoronan muodostumista ja mahdollistivat pernaan kohdennetun mRNA-toimituksen. Prekliinisissä malleissa P1-pohjaiset mRNA-rokotteet laukaisivat voimakkaita vasta-aine- ja T-soluvastauksia, mikä johti merkittävään kasvaimen tukahduttamiseen.
Kliinisten sovellusten mahdollisuudet
Tutkimuksen tulokset korostavat lipidien avaruusrakenteen keskeistä roolia ja tekoälypohjaisten strategioiden potentiaalia optimoida lipidinanopartikkelit elinspesifiseen mRNA-toimitukseen. Tämä voi avata uusia mahdollisuuksia kehittää tehokkaampia ja kohdennetumpia mRNA-pohjaisia hoitoja, erityisesti syövän ja muiden sairauksien hoidossa.
Miksi tämä on tärkeää
Tekoälyn hyödyntäminen lipidien muotoilussa mRNA-toimituksessa voi merkittävästi parantaa hoitojen tehokkuutta ja turvallisuutta. Tämä innovaatio voi mahdollistaa tarkemmin kohdennettuja hoitoja, vähentäen sivuvaikutuksia ja parantaen potilaiden hoitotuloksia. Lisäksi se avaa uusia mahdollisuuksia kehittää mRNA-rokotteita ja -hoitoja, jotka voivat olla ratkaisevia tulevaisuuden lääketieteellisissä sovelluksissa.